6.2.
Кислоты, их свойства и получение
С точки зрения теории электролитической диссоциации кислота – химическое
соединение при диссоциации в воде которого в качестве катионов образуются
только ионы Н+. Представления о кислотах и основаниях, вытекающих из
теории электролитической диссоциации Аррениуса, применимы только для водных
растворов. Исследование процессов, протекающих в неводных средах, без участия
растворителя, потребовало существенных дополнений и привело появлению различных
теорий кислот и оснований.
Различают бескислородные (H2S, HBr, HCl) и кислородсодержащие (H3PO4,
HNO3, HClO3) кислоты.
В свободном состоянии неустойчивы угольная (H2CO3) и
сернистая (H2SO3) кислоты. Различают также сильные (H2SO4,
HNO3, HCl, HBr, HI, HClO4 и др.) и слабые (H2S,
H2CO3, HCN, H2SO3, HClO и др.)
кислоты.
Число ионов водорода, образующихся при диссоциации формульной единицы
кислоты, определяет ее основность.
Названия кислородсодержащих кислот производятся от названия неметалла с
добавлением окончания -ная, -вая, если степень окисления неметалла является
максимальной. По мере понижения степени окисления суффиксы меняются следующим
образом: -оватая, -истая, -оватистая.
Примеры названий некоторых кислородсодержащих кислот приведены в табл.
Таблица Названия некоторых
кислородсодержащих кислот
Формула
кислоты
|
Название
кислоты
|
Формула
кислоты
|
Название
кислоты
|
HClO
|
Хлорноватистая
|
HNO2
|
Азотистая
|
HClO2
|
Хлористая
|
HNO3
|
Азотная
|
HClO3
|
Хлорноватая
|
H2SO3
|
Сернистая
|
HСlO4
|
Хлорная
|
H2SO4
|
Серная
|
Названия бескислородных кислот состоят из названия
неметалла с добавлением соединительной гласной о и слова –водородная. Например:
HF – фтороводородная кислота,
HCl – хлороводородная кислота,
H2S – сероводородная кислота.
1. Большинство кислородсодержащих кислот получают при взаимодействии
кислотных оксидов с водой.
2. Для получения нерастворимых в воде кислот
используют косвенный метод (действием кислоты на соответствующую соль):
Na2SiO3 + H2SO4 → H2SiO3 ↑ + Na2SO4.
3. Некоторые бескислородные кислоты получают при непосредственном соединении
неметаллов с водородом:
H2 + Cl2 → 2 HCl,
S + H2 → H2S.
или по реакции обмена между солью и кислотой:
NaCl + H2SO4(конц) → HCl + NaHSO4
Кислоты представляют собой жидкости (H2SO4, HNO3,
HCl и т.д.) или твердые вещества (H3PO4, H3BO3 и
др.).
Растворы сильных кислот могут разрушать ткани и кожу.
Растворы кислот изменяют цвет индикаторов, что используется для
их качественного обнаружения. В качестве индикаторов используют лакмус (в
нейтральной среде – фиолетовый, в кислой – красный, в щелочной – синий), метилоранж (в
нейтральной среде – оранжевый, в кислой – красный, в щелочной – желтый) и
другие.
Сила бескислородных кислот, например, в ряду HCl – HBr – HI, возрастает с
увеличением радиуса аниона, поскольку анион большего радиуса слабее удерживает
протон, облегчая тем самым диссоциацию кислоты. Таким образом, в главных
подгруппах периодической системы сверху вниз сила бескислородных кислот
возрастает с увеличением радиуса центрального атома.
Наоборот, в ряду HClO – HClO2 – HClO3 –
HClO4 с уменьшением радиуса катиона С1z+ и
увеличением его заряда сила кислородсодержащих возрастает.
Важнейшими химическими свойствами кислот являются:
взаимодействие с основными и амфотерными оксидами, основаниями и солями:
CaO + H2SO4 → CaSO4 + H2O,
ZnO + H2SO4 → ZnSO4 + H2O,
2 Fe(OН)3 + 3 H2SO4 → Fe2(SO4)3 + 6 H2O,
BaCl2 + H2SO4 → BaSO4 + 2HCl;
взаимодействие кислоты с
основанием – реакция нейтрализации;
взаимодействие с
металлами с образованием соли и выделением водорода:
Mg + 2 HCl → MgCl2 + H2,
Fe + H2SO4(разб) → FeSO4 + H2.
Водород из кислот не вытесняют металлы, стоящие в ряду стандартных
электродных потенциалов (в ряду напряжений) правее водорода. При взаимодействии
металлов с концентрированной серной кислотой и азотной кислотой водород как
правило не выделяется.
Концентрированная серная кислота в реакциях с металлами может
восстанавливаться до SO2, S или H2S. Состав продуктов
восстановления определяется активностью металла, концентрацией кислоты и
температурой реагирующей системы. При обычной температуре концентрированная H2SO4 не
реагирует с золотом и платиной, а некоторые металламы (Fe, Cr, Al) пассивируются в
концентрированной серной кислоте.
Малоактивные металлы (стоящие в ряду стандартных электродных потенциалов
правее водорода) восстанавливают концентрированную серную кислоту до SO2:
Cu + 2 H2SO4(конц) → CuSO4 + SO2 ↑+ 2 H2O.
Активные металлы (Ca, Mg, Zn и др.) восстанавливают концентрированную H2SO4 до
свободной серы или H2S:
3 Zn + 4 H2SO4(конц) → 3
ZnSO4 + S ↑ +
4H2O,
4 Ca + 5 H2SO4(конц) → 4 CaSO4 + H2S ↑ + 4H2O.
При взаимодействии
серной кислоты с неметаллами образуется SO2:
C + H2SO4(конц) → 2 SO2↑ + CO2↑ + 2H2O,
S + 2 H2SO4(конц) → 3 SO2↑ + 2H2O,
2 P + 5 H2SO4(конц) → 5 SO2 ↑ + 2 H3PO4 + 2H2O.
При взаимодействии концентрированной H2SO4 с
соединениями, содержащими катионы металлов, находящимися в низшей степени
окисления, происходит дальнейшее окисление этих металлов:
2 FeO + 4 H2SO4(конц) → Fe2(SO4)3 + SO2 ↑ + 4 H2O.
Азотная кислота окисляет большинство элементов до их высшей степени
окисления. Взаимодействие HNO3 различной концентрации с
металлами различной активности представлено в виде следующей схемы:
Разбавленная
|
HNO3
|
Концентрированная
|
||
С тяжелыми металлами
|
С щелочноземельными металлами, а также с Zn, Fe, Sn
|
Не действует на Fe, Cr, Al, Au, Pt
|
С щелочными и щелочноземельными металлами
|
С другими тяжелыми металлами
|
NO
|
NH4NO3
|
N2O
|
NO2
|
Таким образом, при взаимодействии концентрированной HNO3 с
малоактивными металлами образуется NO2:
Ag + 2 HNO3(конц) → AgNO3 + NO2 ↑ + H2O.
При действии разбавленной HNO3 на малоактивные металлы
выделяется NO:
3 Cu + 8 HNO3(разб) → 3 Cu(NO3)2 + 2 NO ↑ + 4 H2O,
а в случае активных
металлов образуется NH4NO3:
4 Ca + 10 HNO3(разб) → 4 Ca(NO3)2 + NH4NO3 + 3 H2O.
При взаимодействии концентрированной азотной кислоты с неметаллами
образуется, как правило, NO:
3 C + 4 HNO3(разб) → 3 CO2 ↑ + 4 NO ↑ + 2H2O,
P + 5 HNO3(разб) + 2 H2O → 3H3PO4 + 5NO ↑.
При взаимодействии концентрированной HNO3 с соединениями,
содержащими катионы металлов, находящимися в низшей степени окисления,
происходит дальнейшее окисление этих металлов:
FeO + 4 HNO3(разб) → Fe(NO3)3 + NO2 ↑ + 2 H2O.
Следует отметить, что продуктами восстановления азотной кислоты с металлами
являются и азот, и даже водород, причем, как правило, образуется смесь веществ.
Чем активнее металл и чем меньше концентрация , тем глубже она
восстанавливается.
Fe*, Аl* с концентрированной азотной кислотой и холодной
концентрированной серной кислотой не реагируют, поэтому данные кислоты
можно перевозить в алюминиевых и стальных цистернах.
Например:
а) с азотной кислотой
10 HNO3(конц.) + 8Na = 8Na NO3 + N2O + 5H2O
4 H NO3(конц.) + Zn = Zn(NO3)2 + 2NO2 + 2H2O
4 H NO3(конц.) + Cu = Cu(NO3)2 + 2NO2 + 2H2O
8 HNO3(разб.) + 3Cu = 3Cu(NO3)2 + 2NO + 4H2O
36 H NO3(разб.) + 10Fe = 10Fe(NO3)3 + 3N2 + 18H2O
9 HNO3(разб.) + 8Na = 8Na NO3 + NH3 + 3H2O
а) с азотной кислотой
10 HNO3(конц.) + 8Na = 8Na NO3 + N2O + 5H2O
4 H NO3(конц.) + Zn = Zn(NO3)2 + 2NO2 + 2H2O
4 H NO3(конц.) + Cu = Cu(NO3)2 + 2NO2 + 2H2O
8 HNO3(разб.) + 3Cu = 3Cu(NO3)2 + 2NO + 4H2O
36 H NO3(разб.) + 10Fe = 10Fe(NO3)3 + 3N2 + 18H2O
9 HNO3(разб.) + 8Na = 8Na NO3 + NH3 + 3H2O
б) с концентрированной
серной кислотой
Zn + 2H2SO4(конц.) = ZnSO4 + SO2 + 2H2O
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S + 4H2O
3Zn + 4H2SO4(конц.) = 3ZnSO4 + S + 4H2O
Сu + 2H2SO4(конц.) = Сu SO4 + SO2 + 2H2O
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S + 4H2O
3Zn + 4H2SO4(конц.) = 3ZnSO4 + S + 4H2O
Сu + 2H2SO4(конц.) = Сu SO4 + SO2 + 2H2O
в) смесь, состоящая из
одной части концентрированной соляной кислоты и трёх частей концентрированной
азотной кислоты растворяет золото. Такая смесь называется
царской водкой.
Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O
Au + HNO3 + 4HCl = H[AuCl4] + NO + 2H2O
УПРАЖНЕНИЯ
1.
Из приведённого перечня выберите кислоты, назовите их,
определите тип.
1) HNO2 2) Li2O 3) H2S 4) CuSO4 5) P2O5 6) Al(OH)3 7) HCl 8) H2SO4
1) HNO2 2) Li2O 3) H2S 4) CuSO4 5) P2O5 6) Al(OH)3 7) HCl 8) H2SO4
Решение:
1) Азотистая кислота – одноосновная,
кислородсодержащая
3) Сероводородная кислота – двухосновная, бескислородная
7) Соляная кислота – одноосновная, бескислородная
8) Серная кислота – двухосновная, кислородсодержащая
3) Сероводородная кислота – двухосновная, бескислородная
7) Соляная кислота – одноосновная, бескислородная
8) Серная кислота – двухосновная, кислородсодержащая
________________________________________________________________
2.
С какими из перечисленных веществ может
реагировать а) HCl б) H2SO4(раствор)
1)Na2O 2)SO3 3)H2O 4) AgNO3 5)HNO3 6)Na2SO4 7)BaCl2 8)Mg 9)Cu 10) NaOH
1)Na2O 2)SO3 3)H2O 4) AgNO3 5)HNO3 6)Na2SO4 7)BaCl2 8)Mg 9)Cu 10) NaOH
Решение:
HCl реагирует с веществами 1,4,8,10
H2SO4 реагирует с веществами 1,4,7,8,10
H2SO4 реагирует с веществами 1,4,7,8,10
________________________________________________________________
3.
Имеются два сосуда,
содержащие 40 и 20 кг раствора кислоты различной концентрации. Если их слить
вместе, то получится раствор, содержащий 33% кислоты. Если же слить равные
массы этих растворов, то полученный раствор будет содержать 47% кислоты.
сколько килограммов кислоты содержится в первом растворе?
Решение:
По известным данным составим пропорцию.
1). 100% - 60 кг
33% - х
кг х=60·33:100=19,8 (кг) - кислоты
содержится всего в двух растворах.
Возьмём по 20 кг каждого раствора, всего будет 40 кг и найдем
сколько там будет содержаться кислоты.
2). 100% - 40 кг
47% - х
кг х=47·40:100=18,8 (кг) - кислоты
содержится в растворах, если взять равные массы.
3). 19,8-18,8=1 (кг) - кислоты осталось в оставшихся двадцати
килограммах раствора. Это как раз первый раствор, содержание кислоты в котором
необходимо узнать.
Так как в двадцати килограммах содержится 1 кг кислоты, то в сорока
килограммах будет содержаться в два раза больше, то есть 2 кг кислоты.
Ответ: 2 кг.
________________________________________________________________
4.
Во что перейдёт сера? Допишите и уравняйте реакции:
(конц.)
Решение:
(конц.)
(концентрированная азотная кислота очень сильный окислитель)
________________________________________________________________
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОГО
РЕШЕНИЯ
1. С
какими из следующих металлов:
- реагирует разбавленная серная кислота? Напишите уравнения реакций в молекулярном и ионном виде.
2. Напишите
уравнения реакций следующих превращений:
3.
Напишите молекулярные и ионные уравнения реакций
между:
а) хлороводородной кислотой и
гидроксидом магния;
б) азотной кислотой и гидроксидом калия;
в) азотной кислотой и гидроксидом цинка;
г) серной кислотой и гидроксидом меди (II).
4. С какими из
следующих веществ будет реагировать соляная кислота:
Напишите уравнения реакций в молекулярной и
ионной формах.
5. С какими из
следующих веществ будет реагировать сернистая кислота:
Напишите
уравнения реакций в молекулярной и ионной формах.
6. С какими из следующих веществ будет
реагировать соляная кислота:
Напишите
уравнения реакций в молекулярной и ионной формах.
7. С
какими из следующих веществ будет реагировать разбавленная серная кислота:
Напишите
уравнения реакций в молекулярной и ионной формах.
8. Сколько граммов
ортофосфорной кислоты получается при растворении 284 г Р2О5
в воде.
9. К 1 л 10%-ного
раствора Н2SO4 (p
= 1,066 г/ мл) добавили 50 г КОН. Какова среда полученного раствора: кислая,
щелочная, нейтральная.
10. На смесь меди и
оксида меди (II) массой 75 г подействовали избытком
концентрированной НNO3. При этом образовался газ объемом 28,88 л
(н.у.). Определите массовую долю оксида меди (II)
в исходной смеси.
|
1.
Формулы только сильных кислот приведены в ряду:
|
|
|
а) HCl, H3PO4,
H2SO4
|
б) H2SO4, H2SO3, HNO3
|
|
в) HNO3, HCl, H2SO4
|
г) HNO2, HNO3, H2SO4
|
|
2.
С какими веществами реагирует соляная кислота:
|
|
|
а) серебром
|
б) силикат калия
|
|
в) оксид кремния (IV)
|
г) сульфат меди (II)
|
|
3.
Непосредственным растворением соответствующих
оксидов в воде нельзя получить
кислоты:
|
|
|
а)ортофосфорную
|
б) кремниевую
|
|
в) азотную
|
г) серную
|
|
4.
В каких парах вещества могут реагировать между
собой:
|
|
|
а) серная кислота и карбонат калия
|
б) нитрат серебра и ортофосфорная
кислота
|
|
в) соляная кислота и железо
|
г) все ответы верны
|
|
5.
Двухосновными кислотами являются:
|
|
|
а) уксусная
|
б) соляная
|
|
в) ортофосфорная
|
г) угольная
|
|
6.
Ортофосфорная кислота не реагирует с:
|
|
|
а) оксидом кальция
|
б) гидроксидом калия
|
|
в) аммиаком
|
г) оксидом кремния (IV)
|
|
7.
Какие кислоты более сильные, чем ортофосфорная
кислота:
|
|
|
а) угольная
|
б) все ответы верны
|
|
в) соляная
|
г) кремниевая
|
|
8.
Укажите формулу самой сильной кислородсодержащей
кислоты хлора:
|
|
|
а) HClO
|
б) HClO3
|
|
в) HClO4
|
г) HClO2
|
|
9.
При внесении каких металлов в разбавленный раствор
серной кислоты выделяется водород:
|
|
|
а) меди
|
б) все ответы верны
|
|
в) цинка
|
г) серебра
|
|
10.
В отличие
от соляной кислоты концентрированная серная кислота при определенных условиях
может реагировать с:
|
|
|
а) гидроксидом калия
|
б) нитратом натрия
|
|
в) оксидом алюминия
|
г) оксидом углерода (IV)
|
Ответы:
|
1
|
в
|
|
2
|
б
|
|
3
|
б
|
|
4
|
г
|
|
5
|
г
|
|
6
|
г
|
|
7
|
в
|
|
8
|
в
|
|
9
|
в
|
|
10
|
б
|



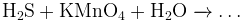









Комментариев нет:
Отправить комментарий