9.6. Диеновые углеводороды (алкадиены).
Каучуки
Алкадиены – алифатически (ациклические), непредельные
(ненасыщенные) углеводороды, с двумя двойными связями в цепи.
Общая формула – CnH2n-2
Алкадиены содержат две
двойные связи в молекуле. В зависимости от взаимного расположения кратных
связей одна относительно другой различают:
а) кумулированные диены:
СН2=С=СН2 аллен
(пропадиен-1,2, кратные связи расположены по соседству):
Можно заметить, что в кумулированных
диенах атом углерода с двумя двойными связями имеет гибридизацию sp, тогда как
соседние с ним углероды – обычную sp2-гибридизацию. Химические
свойства кумулированных диенов резко отличаются от свойств как алкенов, так и
остальных типов диенов.
б) сопряженные алкадиены (или
просто диены; кратные связи расположены через одну простую): СН2=СН-СН=СН2 (бутадиен-1,3), СН3-СН=СН-СН=СН-СН3 (гексадиен-2,4):
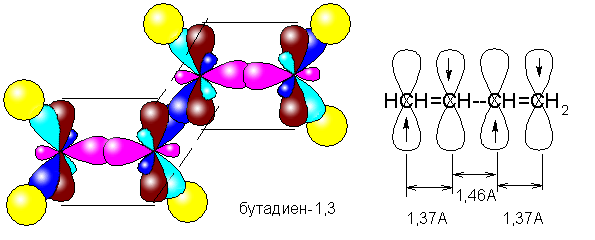
У сопряженных диенов наблюдается
перекрывание соседних р-орбиталей (между атомами углерода, «формально»
разделенными простой связью). Такое перекрывание имеет место в реальности, хотя
в структурных формулах оно не отражается. На самом деле, в молекуле
бутадиена-1,3, например, не существует «чистых» простых или двойных связей, а
все связи «усреднены» и представляют собой нечто среднее между простой и
двойной связью. Такое усреднение не является абсолютным. Длина крайних связей
составляет 1,37 А, а промежуточной – 1,46 А. Напомним, что длина
изолированной двойной связи С=С составляет 1,32 А, а длина простой связи
С-С – 1,54 А.
Вследствие такого взаимодействия орбиталей
появляется даже некоторая энергия стабилизации (резонанса), снижающая
внутреннюю энергию молекулы хоть и на небольшую, но заметную величину в 3-4
ккал/моль (измерено сравнением теплоты гидрирования изолированных и сопряженных
диенов). Это вызывает также некоторые последствия в химических свойствах, о
которых будет рассказано ниже.
в) изолированные диены (кратные
связи разделены более чем одной простой):
СН2=СН-СН2-СН=СН2 (пентадиен-1,4):
Изолированные диены ведут себя как
обыкновенные алкены, поскольку кратные связи не оказывают взаимного влияния в
их молекулах.
Запомнить!
· sp2 гибридизация
· Плоское-тригональное
строение
· Связи
σ и π (вращение относительно двойной С-С связи не возможно)
· Угол HCH =
120 °
0,135 0,148
0,154
· Длина
связи (-С = С – С = С – С – С -)
|
Классификация алкадиенов:
В
зависимости от взаимного расположения двойных связей диены подразделяются на
три типа:
1)
углеводороды с кумулированными двойными связями, т.е.
примыкающими к одному атому углерода.
Например,
пропадиен или аллен CH2=C=CH2
2)
углеводороды с изолированными двойными связями, т.е
разделенными двумя и более простыми связями.
Например,
пентадиен -1,4 CH2=CH–CH2–CH=CH2
3)
углеводороды с сопряженными двойными связями, т.е.
разделенными одной простой связью.
Например,
бутадиен -1,3 или дивинил CH2=CH–CH=CH2
Наибольший интерес представляют углеводороды с сопряженными двойными связями.
Наибольший интерес представляют углеводороды с сопряженными двойными связями.
Физические свойства:
Бутадиен
-1,3 –
легко сжижающийся газ с неприятным запахом, t°пл.= -108,9°C, t°кип.= -4,5°C;
растворяется в эфире, бензоле, не растворяется в воде.
2- Метилбутадиен -1,3 (изопрен) – летучая жидкость, t°пл.= -146°C, t°кип.= 34,1°C; растворяется в большинстве углеводородных растворителях, эфире, спирте, не растворяется в воде.
2- Метилбутадиен -1,3 (изопрен) – летучая жидкость, t°пл.= -146°C, t°кип.= 34,1°C; растворяется в большинстве углеводородных растворителях, эфире, спирте, не растворяется в воде.
Изомерия сопряженных диенов
Структурная изомерия
1. Изомерия положения сопряженных
двойных связей:
2. Изомерия углеродного скелета:
3. Межклассовая изомерия с алкинами
и циклоалкенами.
Например, формуле С4Н6 соответствуют
следующие соединения:
Пространственная изомерия
Диены, имеющие различные заместители
при углеродных атомах у двойных связей, подобно алкенам, проявляют цис-транс-изомерию.
Химические свойства
диеновых углеводородов CnH2n-2
(характерны
реакции горения, присоединения, обесцвечивают водный раствор перманганата калия
и бромную воду)
Реакции присоединения (+Г2; +НГ; +Н2;
+НОН)
|
1. Галогенирование: (образуется смесь продуктов)
а) 1,2-присоединение
б) 1,4-присоединение
(преимущественно)
в) Галогенирование
достаточным количеством галогена:
|
|
2. Полимеризация
nCH2=CH-CH=CH2 t,Na→
(-CH2-CH=CH-CH2-)n
синтетический – бутадиеновый каучук
Элементная ячейка полибутадиена
представляется следующим образом:
Как видно,
образующийся полимер характеризуется транс- конфигурацией элементной
ячейки полимера. Однако наиболее ценные в практическом отношении продукты
получаются при стереорегулярной (иными словами, пространственно
упорядоченной) полимеризации диеновых углеводородов по схеме 1,4-
присоединения с образованием цис- конфигурации полимерной цепи.
Например, цис- полибутадиен
|
Получение алкадиенов
1. Получение бутадиена из
этанола (С.В. Лебедев, 1932).
Этанол пропускают при 400–500 °С над
катализатором из оксилов магния и цинка. Такой катализатор обладает свойством
дегидрировать (окислять) спирты в альдегиды:
а также вызывать конденсацию последнего:
Он же осуществляет и дегидратацию:
Разностороннее действие катализатора
Лебедева позволяло получать в один проход паров спирта над ним бутадиен с
хорошим выходом. Однако протекающие реакции, конечно же, были более сложными.
2. Получение бутадиена
конденсацией ацетилена с формальдегидом (синтез Репе)
Разработанный Репе способ основан на
конденсации ацетилена с формальдегидом:
восстановлении
полученного бутин-2-диола-1,4 в бутандиол-1,4 и дегидратации последнего в
бутадиен-1,3:
Применение
Диеновые углеводороды в основном
применяются для синтеза каучуков:
Натуральный и
синтетический каучуки
Натуральный каучук получают из
млечного сока (латекса) каучуконосного дерева гевеи, растущего в тропических
лесах Бразилии.
При нагревании без доступа воздуха
каучук распадается с образованием диенового углеводорода – 2-
метилбутадиена-1,3 или изопрена. Каучук – это стереорегулярный полимер, в котором
молекулы изопрена соединены друг с другом по схеме 1,4- присоединения
с цис- конфигурацией полимерной цепи:
Молекулярная масса натурального
каучука колеблется в пределах от 7.104 до 2,5.106.
транс - Полимер изопрена также встречается
в природе в виде гуттаперчи.
Натуральный каучук обладает
уникальным комплексом свойств: высокой текучестью, устойчивостью к износу,
клейкостью, водо- и газонепроницаемостью. Для придания каучуку необходимых
физико-механических свойств: прочности, эластичности, стойкости к действию
растворителей и агрессивных химических сред – каучук подвергают вулканизации
нагреванием до 130-140°С с серой. В упрощенном виде процесс вулканизации
каучука можно представить следующим образом:
Атомы серы присоединяются по месту
разрыва некоторых двойных связей и линейные молекулы каучука
"сшиваются" в более крупные трехмерные молекулы – получаетсярезина, которая по
прочности значительно превосходит невулканизированный каучук. Наполненные
активной сажей каучуки в виде резин используют для изготовления автомобильных
шин и других резиновых изделий. Строение резины.
В 1932 году С.В.Лебедев разработал
способ синтеза синтетического каучука на основе бутадиена, получаемого из
спирта. И лишь в пятидесятые годы отечественные ученые осуществили
каталитическую стереополимеризацию диеновых углеводородов и получили
стереорегулярный каучук, близкий по свойствам к натуральному каучуку. В
настоящее время в промышленности выпускают каучук, в котором содержание звеньев
изопрена, соединенных в положении 1,4, достигает 99%, тогда как в натуральном
каучуке они составляют 98%. Кроме того, в промышленности получают синтетические
каучуки на основе других мономеров – например, изобутилена, хлоропрена, и
натуральный каучук утратил свое монопольное положение.
Для вулканизации каучука берётся немного серы 2 – 3 % от общей массы. Если добавить к каучуку более 30 % серы, то она присоединится по линии разрыва почти всех π – связей и образуется жёсткий материал – эбонит.
Для вулканизации каучука берётся немного серы 2 – 3 % от общей массы. Если добавить к каучуку более 30 % серы, то она присоединится по линии разрыва почти всех π – связей и образуется жёсткий материал – эбонит.
О каучуке в стихах
Изделия из натурального каучукаЛетом знойным
Ведут себя довольно непристойно:
Размягчаются, растягиваются,
Липкими бывают,
А морозною зимой
Жесткость и хрупкость приобретают.
Эти недостатки исчезают,
Если каучук в реакцию с серой вступает.
Каучук в резину превращается,
Этот процесс вулканизацией называется.
Макромолекулы между собой
Дисульфидными мостиками «сшиваются».
Если каучук в реакцию с серой вступает.
Каучук в резину превращается,
Этот процесс вулканизацией называется.
Макромолекулы между собой
Дисульфидными мостиками «сшиваются».
Американец Гудьир изобрел вулканизацию в 1839 г.
Серы берется от общей массы процентов 5.
Тогда резина будет эластичностью пленять.
Если же серы 30–50 процентов добавляется,
Твердое, неэластичное вещество получается.
Эбонитом оно называется,
Хорошим электроизолятором является.
Серы берется от общей массы процентов 5.
Тогда резина будет эластичностью пленять.
Если же серы 30–50 процентов добавляется,
Твердое, неэластичное вещество получается.
Эбонитом оно называется,
Хорошим электроизолятором является.
УПРАЖНЕНИЯ
1. Напишите структурные формулы
изомеров диеновых углеводородов состава С5Н8. Назовите
их.
|
__________________________________________________________________
2.
|
__________________________________________________________________
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОГО
РЕШЕНИЯ
1.
Сколько литров (при нормальных условиях) водорода потребуется для гидрирования
смеси из 1,12 л бутена-1 и 2,24 л бутадиена-1,3.
2.
Сколько граммов брома может присоединить смесь, состоящая из 10 г пентана,
7 г пентена-2 и 6,8 г пентадиена-1,4.
3.
Напишите структурную формулу и назовите продукт присоединения HBr к
2-метилбутадиену1,3.
4.
Напишите структурную формулу и назовите продукт присоединения HBr к
2-метилбутадиену1,3.
5.
Напишите структурную формулу и назовите продукт реакции Дильса–Альдера между
бутадиеном 1,3 и этиленом.
6.
Какие соединения получатся после обработки водой продукта взаимодействия
2-метилбутадиена-1,3 и озона? Напишите их структуры.
7.
Какое соединение получится в результате дегидратации бутандиола-1,4 в
присутствии серной кислоты при нагревании.
8.
При бромировании диенового углеводорода получился 2,5-дибромгексен-3. Напишите
формулу исходного диена.
9.
Какой объем этилена (н.у.) потребуется для получения 100 г полиэтилена.
10. При термическом крекинге 8,96 дм3
(н.у.) бутана образуется смесь алкана и алкена с неразветвленной цепью атомов
углерода. Какая масса раствора брома в тетрахлорметане с массовой долей брома
0,05 потребуется для связывания образующегося алкена.
|
1.
Укажите число сигма-связей в молекуле
1.3-бутадиена:
|
|
|
а) 8
|
б) 9
|
|
в) 7
|
г) 5
|
|
2.
Молярная масса алкадиена равна 82 г/моль. Сколько
атомов водорода содержится в молекуле алкадиена:
|
|
|
а) 10
|
б) 12
|
|
в) 14
|
г) 8
|
|
3.
В какой паре оба вещества по отношению друг к
другу являются изомерами:
|
|
|
а) изопрен и 1,3-бутадиен
|
б) винилхлорид и поливинилхлорид
|
|
в) изопрен и пентадиен-1,3
|
г) хлоропрен и винилхлорид
|
|
4.
В молекуле алкадиена 6 атомов углерода. Укажите
значение относительной молекулярной массы алкадиена:
|
|
|
а) 86
|
б) 84
|
|
в) 82
|
г) 80
|
|
5.
Какой продукт преимущественно образуется при
взаимодействии 1 моль 1,3-бутадиена с 1 моль брома при комнатной температуре:
|
|
|
а) 1,4-дибром-2-бутен
|
б) 1,2-дибром-1-бутен
|
|
в) 3.4-дибром-1-бутен
|
г) 1,2,3,4-тетрабромбутан
|
|
6.
При полном гидрировании бутадиена-1,3 образуется:
|
|
|
а) бутен-1
|
б) бутан
|
|
в) изопрен
|
г) бутен-2
|
|
7.
Реакцией Лебедева называется реакция получения:
|
|
|
а) 1,3-бутадиена из этилена
|
б) 1,3-бутадиена из винилхлорида
|
|
в) 1,3-бутадиена из бутана
|
г) 1,3-бутадиена из этанола
|
|
8.
Изопрен можно получить при дегидрировании:
|
|
|
а) метана
|
б) бутана
|
|
в) 2-метилбутана
|
г) 1,3-бутадиена
|
|
9.
При взаимодействии 1 моль водорода и 1 моль
бутадиена-1,3 при комнатной температуре преимущественно образуется:
|
|
|
а) бутан
|
б) бутен-1
|
|
в) бутен-2
|
г) циклобутан
|
|
10.
Бутадиеновый каучук образуется в
результате реакции:
|
|
|
а) дегидрирования бутана
|
б) полимеризации бутена-1
|
|
в) дегидратации и дегидрирования
этанола
|
г) полимеризации 1.3-бутадиена
|
Ответы:
|
1
|
б
|
|
2
|
а
|
|
3
|
в
|
|
4
|
в
|
|
5
|
а
|
|
6
|
б
|
|
7
|
г
|
|
8
|
в
|
|
9
|
в
|
|
10
|
г
|







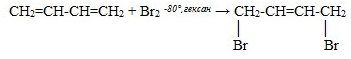






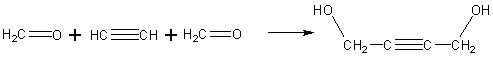














Комментариев нет:
Отправить комментарий